td>
от 40 до 60
-6
более 60
-8
4.
Клиническая эффективность предлагаемого лекарственного препарата статистически значимо выше10 клинической эффективности препарата сравнения, при этом применение лекарственного препарата характеризуется большими затратами, чем применение препарата сравнения12
4.1.
инкрементный показатель "затраты или эффективность" для предлагаемого лекарственного препарата ниже, чем инкрементный показатель "затраты или эффективность" препарата сравнения
более 60
+9
от 40 до 60
+8
от 20 до 40
+7
от 10 до 20
+6
4.2.
инкрементный показатель "затраты или эффективность" предлагаемого лекарственного препарата сопоставим с инкрементным показателем "затраты или эффективность" препарата сравнения
до 10
+5
4.3.
инкрементный показатель "затраты или эффективность" предлагаемого лекарственного препарата выше инкрементного показателя "затраты или эффективность" препарата сравнения
более 60
+1
от 40 до 60
+2
от 20 до 40
+3
от 10 до 20
+4
5.
Клиническая эффективность предлагаемого лекарственного препарата статистически значимо ниже10 клинической эффективности препарата сравнения, при этом применение лекарственного препарата характеризуется меньшими затратами, чем применение препарата сравнения
более 60
+1
от 40 до 60
0
от 20 до 40
-1
от 10 до 20
-2
6.
Клиническая эффективность предлагаемого лекарственного препарата статистически значимо ниже10 клинической эффективности препарата сравнения, при этом затраты на применение лекарственного препарата характеризуются несущественными различиями по сравнению с затратами на препарат сравнения
до 10
-3
7.
Клиническая эффективность предлагаемого лекарственного препарата статистически значимо ниже10 клинической эффективности препарата сравнения, при этом применение лекарственного препарата характеризуется большими затратами по сравнению с затратами на препарат сравнения
от 10 до 20
-4
от 20 до 40
-5
от 40 до 60
-6
более 60
-7
Шкала оценки влияния лекарственного препарата на бюджеты бюджетной системы Российской Федерации14
Результат оценки | Процент отклонения | Шкала оценки (балл) | |
1. | Применение предлагаемого лекарственного препарата приводит к снижению прямых медицинских затрат13 | более 60 | +8 |
от 40 до 60 | +6 | ||
от 20 до 40 | +4 | ||
от 10 до 20 | +2 | ||
2. | Применение предлагаемого лекарственного препарата приводит к несущественному изменению прямых медицинских затрат13 | до 10 | +1 |
3. | Применение предлагаемого лекарственного препарата приводит к увеличению прямых медицинских затрат13 | от 10 до 20 | 0 |
от 20 до 40 | -1 | ||
от 40 до 60 | -2 | ||
более 60 | -4 |
Шкала количественной оценки дополнительных данных о лекарственном препарате
Критерии оценки | Результат оценки | Шкала оценки (балл) |
Необходимость применения лекарственного препарата для диагностики, профилактики, лечения или реабилитации при оказании медицинской помощи в случае заболеваний и состояний, преобладающих в структуре заболеваемости и смертности граждан Российской Федерации, на основании данных государственного статистического наблюдения | да | +2 |
нет | 0 | |
Наличие зарегистрированных в Российской Федерации воспроизведенных лекарственных препаратов | да | +1 |
нет | 0 | |
Наличие лекарственного препарата в перечне стратегически значимых лекарственных средств, производство которых должно быть обеспечено на территории Российской Федерации, утвержденном распоряжением Правительства Российской Федерации от 6 июля 2010 г. № 1141-р | нет | 0 |
да | +1 | |
Наличие лекарственного препарата в перечнях лекарственных препаратов, | нет | 0 |
финансируемых за счет средств бюджетов субъектов Российской Федерации | да | +1 |
Наличие производства (локализация) лекарственного препарата на территории Российской Федерации | нет | 0 |
вторичная упаковка и (или) выпускающий контроль качества - да | +1 | |
| вторичная упаковка и (или) выпускающий контроль качества при наличии заключенного специального инвестиционного контракта, предполагающего создание в Российской Федерации производства готовой лекарственной формы, включая производство фармацевтической субстанции, - да | +2 |
| первичная и вторичная упаковка, выпускающий контроль качества - да | +2 |
| первичная и вторичная упаковка, выпускающий контроль качества при наличии заключенного специального инвестиционного контракта, предполагающего создание в Российской Федерации производства готовой лекарственной формы, включая производство фармацевтической субстанции, - да | +3 |
| все стадии производства, включая производство готовой лекарственной формы (без производства фармацевтической субстанции) , - да | +4 |
| все стадии производства, включая производство готовой лекарственной формы (без производства фармацевтической субстанции) , при наличии заключенного специального инвестиционного контракта, предполагающего создание в Российской Федерации производства готовой лекарственной формы, включая производство фармацевтической субстанции, - да | +5 |
| все стадии производства, включая производство готовой лекарственной формы и производство фармацевтической субстанции, - да | +7 |
| Итоговая оценка прочих данных по предложению (не менее +2 для рекомендации к включению для орфанного лекарственного препарата; не менее +4 для рекомендации к включению остальных лекарственных препаратов с учетом баллов, выставленных главным внештатным специалистом Министерства здравоохранения Российской Федерации в пункте 10 научно обоснованных рекомендаций, приведенных в приложении № 9 к Правилам формирования перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи, утвержденным постановлением Правительства Российской Федерации от 28 августа 2014 г. № 871) . |
_____________________
1 Уровень доказательности результатов клинических исследований применяется для формальной оценки качества отдельного клинического исследования лекарственного препарата. Клинических исследований одного лекарственного препарата может быть несколько, и уровни их доказательности в зависимости от дизайна клинического исследования могут быть различны.
2 Уровень убедительности доказательств эффективности лекарственных препаратов применяется при оценке совокупности исследований одного и того же лекарственного препарата. Осуществляется обобщение данных об уровнях доказательности отдельных исследований различного качества и присваивается один из 3 уровней убедительности.
3 Низкая вероятность ошибок присваивается систематическим обзорам или мета-анализам при соблюдении одновременно следующих условий:
поиск и отбор работ выполнен двумя или более исследователями;
для поиска литературы использовались как минимум 2 электронные библиографические базы данных;
представлена информация о количестве включенных и исключенных работ с указанием причин исключения;
представлена характеристика включенных исследований.
4 Средняя вероятность ошибок присваивается исследованиям любого дизайна в случае отсутствия информации или недостаточности информации по одному или более условиям оценки вероятности возникновения ошибок.
5 Низкая вероятность ошибок рандомизированным клиническим исследованиям присваивается при соблюдении одновременно следующих условий:
рандомизация проводилась на основе случайной последовательности чисел, генерируемой компьютером;
"ослепление" было заявлено или отсутствие "ослепления" не могло повлиять на эффект вмешательства (если изучаемый в исследовании первичный критерий эффективности или безопасности являлся объективным) ;
доля пациентов, выбывших из исследования, составила менее 20 процентов или изучался анализ времени до события (например, общая выживаемость, выживаемость без прогрессирования и др.) ;
представлены результаты по всем запланированным для изучения критериям эффективности и безопасности.
6 Низкая вероятность ошибок сетевых мета-анализов (в том числе непрямых сравнений и смешанных сравнений) присваивается при соблюдении одновременно следующих условий:
в сетевой мета-анализ (в том числе непрямое сравнение и смешанное сравнение) включены только рандомизированные клинические исследования или мета-анализы рандомизированных клинических исследований;
характеристики популяций, вмешательств и общего контроля сопоставимы;
представлено графическое или табличное описание сети доказательств;
приведены результаты отдельных исследований, включенных в сетевой мета-анализ (в том числе непрямое сравнение и смешанное сравнение) .
7 Низкая вероятность ошибок когортным исследованиям присваивается при соблюдении одновременно следующих условий:
когорта является репрезентативной по отношению к изучаемой популяции;
изучаемые когорты отобраны из одной и той же популяции;
подтверждено отсутствие интересующего критерия эффективности или безопасности в начале исследования;
критерии эффективности или безопасности оценивались с помощью независимой оценки (в том числе с ослеплением) или использовались сведения о пациентах из баз данных (регистров) .
8 Низкая вероятность ошибок исследованиям "случай-контроль" присваивается при соблюдении одновременно следующих условий:
группа "случаев" является репрезентативной;
группа "контролей" отбиралась из той же популяции, что и группа "случаев";
подтверждено отсутствие интересующего критерия эффективности или безопасности в начале исследования;
критерии эффективности или безопасности оценивались с помощью независимой оценки (в том числе с ослеплением) или использовались сведения о пациентах из баз данных (регистров) .
9 Высокая вероятность ошибок исследованиям любого дизайна присваивается в случае несоблюдения одного или более условий оценки вероятности возникновения ошибок.
10 При оценке статистической значимости различий в эффективности доверительный интервал не включает 1 (для относительного риска, отношения шансов, отношения угроз) и (или) показатель статистической значимости P<0, 05.
11 При оценке статистической значимости различий в эффективности доверительный интервал включает 1 (для относительного риска, отношения шансов, отношения угроз) и (или) показатель статистической значимости P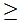 0, 05.
0, 05.
12 В случае если предлагаемый лекарственный препарат не имеет аналогичных лекарственных препаратов в перечнях (представляет собой новый подход к лечению) , инкрементный показатель "затраты или эффективность" для него сравнивается с инкрементным показателем "затраты или эффективность" для лекарственных препаратов, включенных в перечни и применяющихся при заболеваниях из того же класса Международной статистической классификации болезней и проблем, связанных со здоровьем.
Сравниваются инкрементные показатели "затраты или эффективность", рассчитанные на одинаковый клинический эффект (достижение выздоровления, ремиссии, год сохраненной жизни, год сохраненной качественной жизни и др.) .
13 Затраты, связанные с процессом оказания медицинской помощи (затраты на лекарственные препараты, медицинские изделия, медицинские услуги, лабораторные и инструментальные методы исследования, расходные материалы, содержание пациента в медицинской организации или медицинские услуги на дому, транспортировку санитарным транспортом и др.) .
14 Итоговая оценка по результатам оценки экономических последствий применения лекарственного препарата (не менее 6 баллов хотя бы по одному из заявленных показаний) для рекомендации к включению, при этом баллы по шкале клинико-экономической оценки лекарственного препарата и шкале оценки влияния лекарственного препарата на бюджеты бюджетной системы Российской Федерации (далее - бюджет) суммируются. Оценка стоимости курса (года) лечения лекарственным препаратом не влияет на итоговую оценку.
В случае представления заявителем результатов нескольких клинико-экономических исследований в рамках одного показания для определения итоговой оценки выбирается исследование, набравшее наибольший балл.
В случае представления заявителем результатов нескольких исследований влияния на бюджет в рамках одного показания для определения итоговой оценки выбирается исследование, набравшее наибольший балл.
В случае представления заявителем результатов нескольких клинико-экономических исследований по разным показаниям итоговая оценка осуществляется по каждому заявленному показанию.
В случае представления заявителем результатов нескольких исследований влияния на бюджет по разным показаниям итоговая оценка осуществляется по каждому заявленному показанию.".
29. В приложении № 7 к указанным Правилам:
а) в наименовании слова "проведения экспертизы предложения о включении (исключении) лекарственного препарата в перечни лекарственных препаратов" заменить словами "анализа информации о сравнительной клинической эффективности и безопасности лекарственного препарата, оценки экономических последствий его применения";
б) пункт 6 изложить в следующей редакции:
"6. Результаты оценки экономических последствий применения лекарственного препарата:
6.1. расчет стоимости курса (года) лечения предлагаемым лекарственным препаратом по сравнению с лекарственными препаратами, включенными в перечни, указанные в пункте 1.1 настоящего документа, и применяющимися по тем же показаниям, что и предлагаемый лекарственный препарат:
Международное непатентованное наименование | Лекарственная форма | Показание (код Международной статистической классификации болезней и проблем, связанных со здоровьем, расшифровка) | Стоимость годового курса, указанная в предложении заявителем (рублей) | Стоимость годового курса, рассчитанная экспертной организацией (рублей) | Оценка (баллов) для предлагаемого лекарственного препарата |
6.2. результаты клинико-экономической оценки и оценки влияния на бюджеты бюджетной системы Российской Федерации (далее - бюджет) лекарственного препарата по каждому показанию с указанием кода Международной статистической классификации болезней и проблем, связанных со здоровьем, расшифровка:
Клинико-экономическое исследование(анализ влияния на бюджет) | Результат оценки | Оценка (баллов) |
Клинико-экономическое исследование | ||
Анализ влияния на бюджет | ||
| Итоговая оценка по результатам оценки экономических последствий применения лекарственного препарата по показанию"; |
в) пункты 7, 9 и 10 исключить.
30. Дополнить приложениями № 8 и 9 следующего содержания:
"ПРИЛОЖЕНИЕ № 8 к Правилам формирования перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи
(форма)
В Комиссию Министерства здравоохранения Российской Федерации
ЗАКЛЮЧЕНИЕ по результатам анализа методологического качества клинико-экономических исследований лекарственного препарата и исследований с использованием анализа влияния на бюджеты бюджетной системы Российской Федерации, а также изучения дополнительных последствий применения лекарственного препарата
1. Настоящее заключение касается материалов, представленных:
а) для включения лекарственного препарата в следующие перечни:
перечень жизненно необходимых и важнейших лекарственных препаратов для медицинского применения (далее - перечень жизненно необходимых и важнейших лекарственных препаратов) ;
перечень лекарственных препаратов, предназначенных для обеспечения лиц, больных гемофилией, муковисцидозом, гипофизарным нанизмом, болезнью Гоше, злокачественными новообразованиями лимфоидной, кроветворной и родственных им тканей, рассеянным склерозом, а также лиц после трансплантации органов и (или) тканей (далее - перечень дорогостоящих лекарственных препаратов) ;
перечень лекарственных препаратов для медицинского применения, в том числе лекарственных препаратов для медицинского применения, назначаемых по решению врачебных комиссий медицинских организаций (далее - перечень лекарственных препаратов для обеспечения отдельных категорий граждан) ;
б) для исключения лекарственного препарата из перечня жизненно необходимых и важнейших лекарственных препаратов, перечня дорогостоящих лекарственных препаратов и перечня лекарственных препаратов для обеспечения отдельных категорий граждан.
2. Информация об осуществляющих рассмотрение материалов сотрудниках федерального государственного бюджетного учреждения "Центр экспертизы и контроля качества медицинской помощи" Министерства здравоохранения Российской Федерации (далее - Центр экспертизы) включает в себя:
а) фамилию, имя, отчество сотрудника, его должность;
б) адрес Центра экспертизы, телефон (факс) , электронную почту.
3. Информация о лекарственном препарате включает в себя:
а) наименование, в том числе:
международное непатентованное наименование;
в случае отсутствия междун